Victoria Doboș
O echipă de cercetători de la Oxford a realizat un umăr robotic care serveşte ca bioreactor şi mecanism de întindere într-un efort de a creşte, pe cale artificială, ţesut de tendon uman funcţional. În ultimele decenii, oamenii de ştiinţă din domeniul medical au analizat posibilitatea de a utiliza celule fibroblaste pentru a creşte ţesut uman care ar putea înlocui, la pacienţii umani, ţesutul pierdut sau deteriorat. În acest scop, cercetătorii au crescut organe, piele, cartilaj şi chiar o trahee, dar astfel de eforturi se află abia la început.
Un domeniu de cercetare deosebit de provocator este creşterea ţesutului din care este format tendonul. Ţesuturile proiectate până acum nu au demonstrat elasticitatea necesară pentru a putea fi utilizate la pacienţi umani. Pentru a mări elasticitatea ţesutului crescut artificial experţii au încercat să construiască dispozitive care să întindă şi să îndoaie ţesutul pe măsură ce acesta creşte. Din păcate, aceste încercări nu au produs ţesut care să se îndoaie, să se răsucească şi să se întindă la fel cum o face ţesutul natural.
În acest nou efort, cercetătorii de la Oxford au adoptat o nouă abordare. În loc să cultive ţesutul în vase Petri cu dispozitive de întindere, oamenii de ştiinţă au crescut ţesutul pe o articulaţie fabricată în aşa fel încât să imite un umăr uman.
Ministerul Sănătăţii urmează să introducă 7 noi protocoale terapeutice, în urma adăugării unor medicamente pe lista tratamentelor compensate, şi să actualizeze 17 protocoale existente, la recomandarea comisiilor de specialitate. Măsura este cuprinsă într-un proiect de ordin comun al ministrului Sănătăţii şi al preşedintelui Casei Naţionale de Asigurări de Sănătate (CNAS). Astfel, noul ordin introduce 7 noi protocoale terapeutice, pentru selexipag (medicament indicat terapeutic pentru hipertensiune arterială pulmonară), lanadelumab (angioedem ereditar), tolvaptan (hiponatremie secundară sindromului de secreţie inadecvată de hormon antidiuretic), ketoconazol (sindromul Cushing), risdiplam (atrofie musculară spinală), combinaţii beclometazonă + formoterol + glicopironiu (boală pulmonară obstructivă cronică – BPOC, astm bronşic) şi combinaţii formoterol + glicopironiu + budesonidă (BPOC). De asemenea, actul normativ prevede actualizarea a 17 protocoale terapeutice. Protocoalele terapeutice au fost analizate şi avizate de către Agenţia Naţionala a Medicamentului şi a Dispozitivelor Medicale din România (ANMDMR). Potrivit legislaţiei, prescrierea, eliberarea şi decontarea medicamentelor în sistemul public de asigurări de sănătate se realizează şi în baza protocoalelor terapeutice aprobate prin ordin comun al Ministerului Sănătăţii şi al CNAS.
Coriandrul face parte din familia Apiaceae, fiind o plantă erbacee, anuală, cultivată şi sporadică, cu frunze glabre, lucioase, de culoare verde-deschis. Florile sunt mici, albe, roz sau violete, grupate în inflorescenţe, iar fructele se gasesc sub forma de globuleţe, fiind bogate în uleiuri volatile. Originar din Asia şi Orient, coriandrul este cunoscut şi folosit în medicina tradiţională din vremuri îndelungate. Istoria utilizării acestei specii medicinale are mai mult de trei mii de ani, seminţele extrem de parfumate ale coriandrului, cu o aromă undeva între cea de citrice şi cea a lăcrămioarelor, fiind intens utilizate în scopuri medicinale şi magice de către egipteni, greci şi mai apoi romani. Se mai numeşte buruiana pucioasă, coleandră, iarba puturoasă, piper alb, pucioasă, puturoasă etc. Acţiuni INTERN: tonic digestiv, stomahic, carminativ, antispastic, bactericid, fungicid, sedativ, anxiolitic, afrodisiac, antiinflamator, vermifug. EXTERN: antimicrobian, antiinflamator. Indicaţii INTERN: se utilizează ca adjuvant în: anorexie, dispepsii, indigestie, meteorism (balonare), colite, colici abdominale la copii, anxietate, artrite, reumatism, helmintiaze (viermi intestinali). EXTERN: se utilizează ca adjuvant în: artrite, reumatism, plăgi (impiedică suprainfectarea rănilor).
Despre uleiul de peşte s-au scris multe lucrări. Se ştie că uleiul de peşte este esenţial pentru dezvoltarea sănătoasă a copilului, pentru dezvoltarea sănătoasă a organismului. Istoria uleiului de peşte şi a beneficiilor acestuia are o vechime de mii de ani. Este considerat din timpuri străvechi un adevărat dar al naturii de către locuitorii zonelor arctice şi sub-arctice. Era folosit la aproape orice: de la iluminat lămpile, prelucrarea pieilor de animale, tratarea bărcilor şi a corăbiilor pentru a preveni acoperirea lor cu gheaţă până la folosirea lui ca medicament, atât pentru oameni cât şi pentru animale. Primele dovezi despre beneficiile uleiului de peşte datează de pe vremea vikingilor, iar în nordul Norvegiei s-au găsit dovezi ale folosirii uleiului de peşte iîn scopuri medicinale din perioada 230-895 (d.Hr.). Explicaţia e simplă. Pentru a supravieţui în condiţiile aspre din nord, cu lipsa soarelui pe perioada iernii (deci şi a vitaminei D) localnicii au învăţat repede că, luat zilnic, uleiul de peşte este un remediu excelent pentru sănătate în general dar şi pentru a preveni rahitismul sau afecţiunile reumatismale. Primele atestări medicale ştiinţifice datează din 1789, şi ele au fost descoperite în Manchester, când Dr. Darbey a folosit ulei de peşte pentru a trata reumatismul. Legat de beneficiile uleiului de peşte sau a uleiului extras din ficat de cod, Peter Möller a observat că locuitorii de pe coasta de vest a Norvegiei se îmbolnăveau foarte rar, datorită consumului frecvent de ulei de ficat de cod. Pornind de la această bază, s-a dedicat cercetării şi identificării metodelor de a produce ulei de ficat de cod cu gust mai bun, de o puritate mai mare. Astfel, a dezvoltat şi patentat metoda utilizării aburului de a extrage uleiul din ficatul de cod proaspăt, păstrându-se astfel substanţele nutritive. Se ştie deja că uleiul de peşte este atât de sănătos datorită conţinutului ridicat de acizi graşi Omega 3.
Creierul şi organele de reproducere masculine par că pot alege mai multe secvenţe diferite de cod genetic pentru a produce o anumită proteină. Oamenii de ştiinţă spun că utilizarea acestor secvenţe rare de cod genetic ar putea reprezenta un alt nivel de control în genom, esenţial pentru fertilitate şi evoluţie.
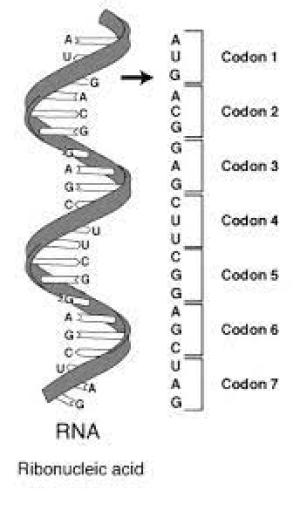
La un deceniu de la descifrarea structurii ADN, spirala dublă formata din patru baze azotate, A (adenina), C (citozina), G (guanina) şi T (timina), britanicul Francis Crick a continuat cercetările pentru a descifra secvenţele intermediare, respectiv modul în care trei dintre aceste baze azotate dintr-o genă sunt transpuse în codon, o secvenţă intermediară formata doar din trei nucleotide, care reprezintă „reţeta” pentru formarea unui singur aminoacid, principalul bloc de construcţie al unei proteine.
Ceea ce a fost izbitor la momentul respectiv şi a rămas încă oarecum o enigmă, este faptul că acest nivel din ADN a folosit 61 de codoni de trei litere diferiţi pentru a produce doar 20 de aminoacizi, ceea ce înseamnă că mulţi codoni au fost sinonimi, descriind aceleaşi informaţii.
„Suntem învăţaţi la orele de biologie ca atunci când trecem de la o versiune la alta a codonului şi aminoacidul nu se schimbă, avem de-a face cu ceea ce se numeşte o mutaţie tăcută. Adică, mutaţia nu contează. Cu toate acestea, atunci când cercetătorii au secvenţiat organisme diferite, au identificat o ierarhizare, unii codoni fiind exprimaţi foarte frecvent, iar alţii foarte rar. Această distribuţie a codonilor poate varia între diferitele tipuri de ţesut şi de la un organism la altul“, a declarat lect univ. dr. Don Fox, profesor de farmacologie şi biologie a cancerului la Duke School of Medicine.
Cercetătorii de la facultatea de medicină din Missouri au descoperit o imunoterapie combinată care se arată promiţătoare în lupta împotriva cancerului de ficat.
Terapia constă dintr-o moleculă de lipide care suprimă tumorile, numită nanolipozom cu ceramida C6 (LipC6) şi un anticorp pentru antigenul citotoxic al limfocitelor T (CTLA4). Când LipC6 şi anticorpul anti-CTLA4 au fost folosite împreună au încetinit semnificativ creşterea tumorii şi au îmbunătăţit rezistenţa celulelor T care atacă tumorile, au declarat cercetătorii. „Analiza noastră a arătat că terapia combinată a extins semnificativ durata de viaţă a şoarecilor cu tumori în comparaţie cu şoarecii cu un singur tip de terapie sau fără nicio terapie“, a declarat unul dintre cercetătorii principali, lector univ. dr. Guangfu Li, profesor în cadrul departamentului de chirurgie şi microbiologie moleculară şi imunologie.
În opinia cercetătorilor, această constatare este deosebit de promiţătoare, având în vedere că în prezent lipsesc terapiile eficiente împotriva cancerului hepatic, care reprezintă a treia cauza de decese legate de cancer în SUA. Rata medie de supravieţuire de cinci ani a pacienţilor diagnosticaţi cu cancer hepatic este de 20%, potrivit Societăţii Americane de Cancer.
Leurda este o plantă erbacee cu miros şi gust de usturoi. Face parte din familia liliaceelor. Înălţimea maximă pe care o poate atinge este de un metru şi jumătate. În pământ, leurda are un bulb ovoidal, format din solzi groşi, asemănători căţeilor de usturoi. Tulpina este însoţită de două frunze. Leurda înfloreşte în aprilie şi mai, uneori şi in iunie. Florile se adună într-o inflorescenţă sub formă de umbrelă, ce cuprinde între cinci şi 20 de flori de un alb strălucitor. Fructul este o capsulă. Leurda poate înlocui usturoiul şi poate fi conservată. Creşte în toate zonele României. Din punct de vedere medicinal, importante sunt frunzele – din care se prepară o infuzie. Leurda are virtuţi antiscorbutice, depurative, diuretice, tonificatoare. Este recomandată în avitaminoze. Este şi un agent eficient de curăţire a organismului, a tractului gastro-intestinal şi nu numai, în reglarea activităţii rinichilor, precum şi în activarea şi reactivarea activităţii intestinale.
Cercetători de la colegiul medical al universităţii Augusta, din Statele Unite, au identificat în testul standard pentru mielomul multiplu, indicii clare care arată dacă pacientul are una dintre cele mai neobişnuite şi mortale forme ale acestui tip de cancer. Un tip rar de cancer de sânge, mielomul cu imunoglobulina D (IgD), reprezintă 1% dintre mieloamele multiple şi are un prognostic mai slab.
Dr. Gurmukh Singh, autorul studiului publicat în International Journal of Pathology and Clinical Research a declarat că deşi există un test specific pentru diagnosticarea mielomului multiplu IgD, indiciile din testele standard pot fi suficiente pentru a iniţia rapid un tratament agresiv care să reducă sau să prevină distrugerea rinichilor din cauza numărului excesiv de proteine circulante monoclonale (lanţuri uşoare), pe care acest cancer le produce. Investigaţiile specifice pentru IgD sunt disponibile doar la câteva laboratoare de referinţă şi necesită timp şi cheltuieli suplimentare care probabil că vor întârzia începerea tratamentului şi ar putea să nu fie necesare, a precizat medicul, care este şi vicepreşedintele departamentului de patologie al colegiului medical din Georgia.
În acest tip de cancer, celulele plasmocitare, care produc în mod normal o gamă larga de anticorpi pentru a ajuta organismul să lupte împotriva infecţiilor, fiind maligne, provoacă manifestări neobişnuite şi produc un singur anticorp disfuncţional, numit spike-M, care lasă organismul vulnerabili la infecţii şi poate ataca chiar şi oasele, explică dr. Singh.
Pelinul este „oaia neagră” a plantelor medicinale, fiindcă gustul său amar foarte intens este suportat şi plăcut de puţine persoane. Este însă un puternic detoxifiant, pe care îl putem include din când în când în dieta noastră. Ceaiul de pelin se realizează din frunze şi tulpini uscate, o lingură plină adăugată în 25-300ml apă clocotită. Se acoperă şi se lasă la infuzat 5-10 minute. Se strecoară şi se poate bea cât este călduţ. Deşi gustul poate fi greu de suportat, este de preferat să nu îndulceşti ceaiul cu zahăr. Poţi adăuga o linguriţă de miere şi 2-3 picături de lămâie, care îi vor schimba puţin aroma.
Poţi bea o cană cu ceai de pelin cu o jumătate de ora înainte să iei micul dejun. În acest mod, infuzia îşi va face efectul, iar mâncarea consumată după te va scăpa de gustul neplăcut cu care rămâi. Înainte de a discuta despre beneficiile ceaiului de pelin, trebuie să ştii că nu este recomandat femeilor însărcinate şi celor care alăptează, precum nici persoanelor care suferă de boli ale sistemului nervos. De asemenea, nici persoanele cu afecţiuni cardiace nu ar trebui să consume ceai de pelin întruct acesta poate încetini ritmul cardiac. Nici pacienţii cu astm alergic nu ar trebui să consume ceai de pelin, iar cei cu dermatită de contact nu ar trebui să aplice acest ceai la nivel cutanat întrucât poate declanşa iritaţii. În plus, este extrem de important să nu bei ceai de pelin mai mult de două săptămâni, fiindcă poate avea efecte secundare ca halucinaţiile, convulsiile, vărsăturile şi ameţelile.
Conf. dr. Diana Păun, consilier de stat la Departamentul Sănătate Publică al Administraţiei Prezidenţiale, participă la dezbaterea online ,,Multiple Sclerosis360”, organizată de redacţia 360medical.ro, un eveniment din seria conferinţelor 360 APT, Acces, politici şi terapii, care va avea loc astăzi începând cu ora 18. Manifestarea se desfăşoară pe parcursul a două zile, respectiv 26 şi 27 mai 2022 şi marchează Ziua Mondială de Scleroză Multiplă, ce va fi celebrată pe 30 mai.
Tema Federaţiei Internaţionale de Scleroză Multiplă aleasă pentru Ziua Mondială de Scleroză Multiplă ,,Mă conectez. Ne conectăm” îşi propune să atragă atenţia asupra abordării holistice şi multidisciplinare a persoanelor cu scleroza multiplă (SM).
Conf. Univ. Dr. Diana Loreta Păun va transmite în cadrul evenimentului mesajul Administraţiei Prezidenţiale pentru persoanele cu SM din România şi pentru cei care le oferă îngrijiri medicale. Actualmente, cel puţin 1,8 milioane de persoane cu SM, ceea ce reprezintă două treimi din populaţia mondială de pacienţi cu această afecţiune, trăiesc în ţări care nu au orientări naţionale pentru diagnosticarea şi tratamentul SM şi nu dispun de ghiduri naţionale şi standarde naţionale pentru îngrijirea SM.
Potrivit celei de-a treia ediţii a Atlasului de SM al Federaţiei Internaţionale de Scleroză Multiplă, exista variaţii uriaşe la nivel mondial în ceea ce priveşte numărul de neurologi la 100.000 de persoane, variind de la o prevalenţă mediană de 4,6 neurologi la 100.000 de persoane în ţările cu venituri ridicate la 0,05 în ţările cu venituri mici.
Cele mai citite
Error: No articles to display